



Artículos
Análisis macrocinético de la infiltración química de vapor de capas de Si y Si/SiC en estructuras biomórficas de carbono
ACI Avances en Ciencias e Ingenierías
Universidad San Francisco de Quito, Ecuador
ISSN: 1390-5384
ISSN-e: 2528-7788
Periodicidad: Bianual
vol. 1, núm. 1, 2008
Publicación: 01 Abril 2009

Resumen: En este artículo se presenta el modelo matemático desarrollado para describir y predecir el proceso de in- filtración y deposición de capas de Si y Si/SiC a partir de los sistemas de precursores: metiltriclorosilano (MTS)/hidrógeno y Tetracloruro de Silicio/hidrógeno. Este modelo se basa en la cinética obtenida en el análisis experimental de la deposición sobre substratos no porosos, en el modelo geométrico desarrollado para describir la estructura porosa de las preformas de carbono y en el cálculo de Módulo de Thiele y del factor de infiltración a partir del balance de masa. Finalmente se comprobaron los resultados del modelo matemático comparando la homogeneidad de la infiltración en preformas de carbono con un microscopio SEM.
Palabras clave: Chemical Vapor Deposition (CVD), CVI, biomorphic ceramics, infiltration factor.
Introducción
El desarrollo en las técnicas de producción de cerámicas biomórficas aumenta continuamente [1]. Cerámicas biomórficas son materiales tecnológicos obtenidos de la transformación de estructuras biológicas, llamadas pre- formas, hacia materiales cerámicos de alta calidad y una amplia gama de posibles aplicaciones1. Las cerámicas biomórficas de carburo de silicio, SiC, han sido estudiadas exhaustivamente por su combinación única de pro- piedades. SiC se caracteriza por su muy buena resistencia mecánica, estabilidad térmica hasta 1000°C en atmósferas oxidantes y su resistencia química a ácidos y bases. Entre sus principales aplicaciones se encuentran su uso como monolito o recubrimientos en motores y partes que necesitan resistencia a altas temperaturas, o como protección a medios abrasivos o corrosivos [2, 3]. Entre las propiedades únicas de las estructuras biológicas se encuentran la combinación entre resistencia y estabilidad con gran flexibilidad y elasticidad, densidades muy bajas, además de su posibilidad de auto- curación y auto-modificación, cosa que no se tiene en ningún material tecnológico [4, 5]. Las propiedades únicas de las cerámicas biomórficas de SiC son una combi- nación entre las propiedades cerámicas del SiC y de la estructura original biológica, la cual se mantiene intacta hasta un nivel de micrométrico, resultando en materiales de bajísima densidad y alta flexibilidad, con alta resistencia mecánica y dureza, así como alta estabilidad, conductividad térmica y resistencia química frente a ácidos y bases [6,7].
En los últimos años se han desarrollado diferentes tecno- logías para la obtención de cerámicas biomórficas, dan- do como resultado cerámicas con diferentes propie- dades. Las tecnologías más utilizadas son infiltración de Si líquido [8,9, 10], infiltración de Si gaseoso [11, 12], infiltración de vapor de SiO [11] e infiltración química
de vapor [13, 14, 15]. En este trabajo va a tratar exclusivamente cámicas biomórficas producidas a través de la deposición e infiltración química de vapor (CVI, Chemical Vapor Infiltration) de diferentes precursores
El proceso de ceramización por el método de CVI inclu- ye tres pasos consecutivos [16]. En el primer paso se transforma la estructura biológica en la preforma de car- bono por una reacción de pirólisis [1, 14, 17, 18]. El papel utilizado fue especialmente diseñado para este proceso de ceramización, basado únicamente en fibras gruesas de celulosa y lignina para mantener una gran porosidad de la estructura.
En el segundo paso la preforma de carbono es sometida al proceso de CVI, donde es infiltrada con el precursor en fase gaseosa a la temperatura de reacción. Los sistemás de reacción que se van a estudiar en este trabajo son: metiltriclorosilano (MTS) – hidrógeno (CH.SiCl.- H.) y tetracloruro de silicio – hidrógeno (SiCl.-H.). El depósito sólido que se obtiene con los diferentes siste- mas es Si/SiC y Si respectivamente.
El tercero y último paso consiste en la reacción en fase sólida del Si depositado con el carbono de la preforma y la combustión del carbono en exceso, para finalmente obtener la cerámica biomórfica deseada de SiC.
Este trabajo se va a enfocar en el segundo paso descrito: la ceramización por el método de CVI. Se realizará un análisis macro-cinético del mecanismo de infiltración de los precursores en fase gaseosa a través de la preforma de carbono hasta depositarse como un recubrimiento sólido en toda su superficie interior. Con este modelo se quiere predecir la homogeneidad del depósito a lo largo de la estructura porosa. Para poder realizar este análisis es de vital importancia conocer la cinética química del proceso de deposición. Para esto se realizaron investigaciones previas a la infiltración sobre substratos no porosos, hasta obtener una ecuación cinética del proceso de deposición. A continuación, se establece un modelo para la infiltración y la deposición en los substratos porosos.
Por consiguiente, este trabajo va a estar dividido en tres partes. En la primera parte se presentarán los resultados del estudio cinético de la deposición química de vapor en sustratos no porosos. En la segunda parte se presentará el modelo matemático que se ha desarrollado sobre la geometría de la preforma. Y por último se combinará el modelo geométrico con la expresión cinética, para formular el modelo matemático que representa la infiltración de los gases reactivos y la deposición en la pre- forma de carbono. Finalmente se comprobarán los resultados matemáticos con las pruebas cerámicas.
Materiales y métodos
a) Equipo experimental
El equipo utilizado para la infiltración química de vapor es un reactor tubular para deposición química de vapor (CVD, Chemical Vapor Deposition) de calentamiento térmico por conducción en la pared. Los gases reactivos e inertes son dosificados por controladores de flujo másico. El precursor líquido, MTS o SiCl., es evaporado y transportado por un gas inerte (helio) desde un evaporador temperado hasta el reactor. Al regular la tempera- tura del evaporador y el flujo del gas de arrastre se pue- de conocer, con ayuda de la curva de presión de vapor del precursor, la cantidad de este que es introducida el reactor. En este tipo de reactor los gases introducidos llegan a la temperatura de deposición en la fase gaseosa y se forma el depósito en todas las superficies calientes. Es por esto por lo que el reactor tubular está protegido por un folio de grafito a lo largo y ancho del mismo. Las pruebas de grafito y las preformas de carbono son colocadas al inicio de la zona isotérmica del reactor donde se ha observado una deposición homogénea [14].
b) Análisis cinético en procesos de CVD / CVI
La deposición química de vapor es un proceso complejo que involucra por el lado cinético una serie de reacciones en fase gaseosa donde se forman los reactivos inter- medios, seguidas por las reacciones heterogéneas en fase sólida, donde se forman la capa sólida deseada y los productos gaseosos finales.
Por lo tanto, los pasos elementales para la formación del depósito son: difusión de película ocasionada por limitaciones en la convección del gas reactivo hasta la superficie del substrato, adsorción y reacción superficial formando la capa sólida, más los pasos de desorción y difusión de película de los productos secundarios.
En el caso de substratos porosos se debe incluir antes del paso de adsorción y después de la desorción adicional- mente la difusión de los precursores o los productos secundarios por los poros o infiltración. Se desea operar de tal forma, que la infiltración y deposición sea homogénea en todo el substrato [19,20].
Todos estos pasos ocurren en serie y, por lo tanto, el más lento de éstos es responsable de la velocidad global del proceso. Es por esto que es de suma importancia analizar en cuál régimen de parámetros se tiene una deposición o infiltración controlada por la reacción superficial, ya que sólo bajo estas condiciones se tiene una infiltración homogénea del gas reactivo y se puede formar una capa sólida homogénea en todo el substrato poroso.
Los principales parámetros que se deben controlar y modificar para lograr la deposición e infiltración desea- da son temperatura de deposición, velocidad del gas en el reactor, presión total y composición de gases reactivos.
Por lo general, se encuentran procesos controlados por difusión de película a altas temperaturas, y presiones y velocidad del gas bajas, lo que ocasiona una película gaseosa ancha y difícil de difundir, y al mismo tiempo una reacción cinética rápida, pero con baja concentra- ción de precursor en la superficie. Por el otro lado, a temperaturas y presiones bajas y tiempos de residencia más cortos, la velocidad de reacción es el paso más lento y controla el proceso general. En substratos porosos se debe incluir además la limitación por difusión de poros. En este caso el paso limitante se define por la geometría del substrato y por las condiciones de difusión del gas: temperatura, presión total y presiones parciales de los precursores.
Para realizar el análisis cinético se estudiarán tanto la dinámica de fluidos, la cinética de la reacción de deposi- ción en substratos no porosos y finalmente la cinética en substratos porosos.
La dinámica de fluidos incluye transporte de masa y de calor por convección y conducción, y explica su com- por-tamiento en el reactor. El principal método expe- rimental para la determinación de las condiciones de dinámica de fluidos del proceso de deposición es anali- zar la velocidad de reacción y el tiempo de residencia del gas reactivo en el reactor. En tiempos de residencia pequeños se encuentra una dependencia lineal entre el mismo y la conversión del gas reactivo en un depósito sólido. Este régimen se encuentra controlado por el flujo forzado o convección y se lo conoce como feed rate limitation. Este régimen se caracteriza por tener tiempos de residencia del gas muy cortos, los cuales no alcanzan a reaccionar completamente en el reactor. Al seguir aumentando el tiempo de residencia del gas se llega des- pués de un inter-valo de transición a un régimen en el cual la conversión es independiente del tiempo de resi- dencia. En este régimen la reacción superficial controla el mecanismo de deposición. Esta conversión es al mis- mo tiempo la conversión máxima que se alcanza en el proceso y es el régimen de operación deseado. Si se continúa aumentando el tiempo de residencia, la conver- sión empieza a disminuir. Éste es el régimen de limita- ción por difusión de película del gas reactivo en las su- perficies del reactor: paredes y substratos a depositar.
Otros criterios para conocer la dinámica de fluido duran- te el proceso de deposición son el cálculo de números adimensionales como los números de Reynolds, de Knudsen o de Damkohler. En este trabajo no se los tra- tará a detalle, pero se puede encontrar su aplicación en Almeida [1].
La cinética en procesos de CVD es compleja e involucra una serie de reacciones homogéneas en fase gaseosa y reacciones heterogéneas en fase sólida, incluyendo pro- cesos de adsorción, desorción y reacción superficial que forman la capa sólida deseada [20]. Sin embargo, la cinética de la deposición se puede expresar como una sola expresión global.
Los experimentos para la obtención de los datos cinéti- cos en substratos no porosos se realizaron en el régimen de deposición determinado por la reacción cinética. Se asume para la velocidad de reacción un modelo de ley de potencia y se utilizan únicamente los datos experi- mentales al principio de la zona isotérmica del reactor para obtener los datos cinéticos deseados y minimizar el efecto de los productos gaseosos inhibidores, como HCl.
 [Ecn. 1 Ecn. 2]
[Ecn. 1 Ecn. 2]En Ecn. 1 y Ecn. 2 se presentan la forma de la l1ey de potencia de la velocidad de reacción y la forma lineali- zada logarítmica de la cual se obtiene el orden de reac- ción, n. Experimentalmente se conoce la velocidad de reacción superficial, r., en [mol/m2.s], a través de la ma- sa depositada en cada substrato de área conocida en el tiempo definido por la duración de experimento, y la concentración de precursor en cada posición del reactor, Cprec, en [mol/m3] [1]. Con estos datos se obtiene de la pendiente de la curva de log(r.) vs log(Cprec) el orden de la reacción. Mientras que el coeficiente cinético, k., se obtiene despejando k. de Ecn. 2.
En el siguiente paso se obtiene la energía de activación de la reacción superficial, E., y el coeficiente preexpo- nencial, k., utilizando la forma logarítimica de la ley de Arrhenius de Ecn. 3. La validación de los datos cinéticos se asegura con extrapolación de datos en diagramas de paridad con ± 20% [1].
 [Ecn. 3]
[Ecn. 3]c) Cálculo del factor de infiltración en procesos de CVI
Los modelos matemáticos en procesos de CVI son nece- sarios para proveer un mejor entendimiento de la in- fluencia de los parámetros individuales sobre las propie- dades del material final, en especial con respecto al per- fil de deposición en toda la estructura porosa y la poro- sidad final. Realizar un modelo realista de la CVI resul- taría muy complicado debido a la estructura indefinida de los poros del substrato a infiltrar. Es por esto que se realiza modelos simplificados de los procesos de deposi- ción e infiltración. Primero se necesita determinar un modelo de la geometría de los poros, para en el siguiente paso poder establecer un balance de masa en los poros y después poder calcular la velocidad de reacción efectiva a lo largo del poro.
Una vez obtenidos los términos de la reacción cinética superficial y la velocidad de reacción efectiva en subs- tratos porosos es posible calcular el factor de infiltración al relacionar los dos términos (reff/r.). El factor de infil- tración ( ) en los poros indica el grado de difusión de los gases dentro de la estructura sólida y la homogeneidad de las capas formadas. Por lo tanto, un factor de infiltración cercano a 1 indica que la difusión es rápida comparada con la reacción cinética y que las capas son homogéneas, mientras que un factor de infiltración me- nor a uno indica que la difusión en la estructura no es homogénea y que, por lo tanto, el recubrimiento en el centro de la preforma va a ser deficiente.
d) Métodos de caracterización
Mediante scanning electron microscopy (SEM/EDX Phillips XL 30) y espectroscopía Raman (Raman Spec- trometer Type Renishaw Ramascope 2000) se puede validar los resultados del modelo matemático al comprobar la homogeneidad en la deposición de las prefor- mas obtenida con la esperada [1].
Resultados y discusión
a) Análisis cinético de la deposición química de vapor de los sistemas MTS - H2 y SiCl4 - H2
La expresión cinética para la velocidad de deposición de las capas cerámicas de Si/SiC y Si, se obtiene experi- mentalmente haciendo series de experimentos de la de- posición química de vapor en substratos no porosos y variando ciertos parámetros.
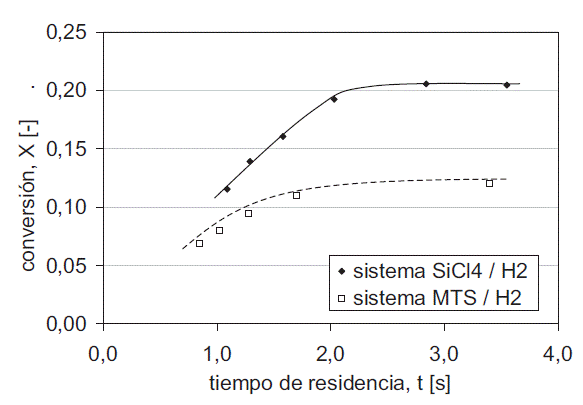
En esta serie de experimentos el primer paso es determi- nar el régimen en el flujo del precuror en el cual la velo- cidad de deposición sea determinada por la reacción cinética superficial. Como descrito anteriormente, este régimen se encuentra en tiempos de residencia entre la limitación por convección y la limitación por difusión de película. Entre estos dos regímenes se encuentra el tiem- po de residencia de los gases, en el cual el proceso de deposición está determinado por la reacción cinética. La conversión alcanza su máximo y es independiente del tiempo de residencia. En la Figura 1 se muestran los resultados de los experimentos de variación del tiempo de residencia del gas,para conocer las condiciones de operación donde el pro- ceso se encuentra controlado por la reacción superficial. Esto es cuando la conversión es independiente del tiem- po de residencia. En los sistemas MTS/H. y SiCl./H. los tiempos de residencia óptimos se encuentran en 1,7 y 2,0 s, respectivamente.
| Parámetros Sistema MTS / H2 SiCl4 / H2 temperatura [°C] 800 - 1000 850 - 1050 presión total [mbar] 1000 1000 tiempo de residencia [s] 0,8 - 3,5 1,0 - 3,5 fracción molar de precursor 1 [-] 0,01 - 0,10 0,01 - 0,08 fracción molar de precursor 2 [-] - - relación H2 / precursor [-] 0 - 90 1 - 99 |
| Datos cinéticos | Sist / | ema l / |
| MTS H2 | SiC 4 H2 | |
| Factor preexponencial, k0 [cm/s.(mol/cm3)1-n] | 3,30E+04 | 5,23E+04 |
| Energía de activación, Ea [kJ/mol] | 174 | 191 |
| Orden de reacción, n1 [-] | 0,61 | 0,64 |
Una vez determinado el flujo volumétrico óptimo de los gases reactivos, se inicia con la variación de las demás condiciones de operación: temperatura, presión, concen- tración de los reactivos. Y utilizando la metodología explicada anteriormente se obtienen los valores de los parámetros cinéticos. La Tabla 1 muestra el rango de variación de las condiciones de operación en los sistemas estudiados. Y en la Tabla 2 se encuentran los resul- tados obtenidos del análisis cinético.
b) Cálculo del factor de infiltración
El modelo matemático desarrollado en este trabajo para predecir el factor de infiltración mediante CVI en las preformas de carbono se basa en un modelo unidimen- sional, considerando los cambios en la porosidad duran- te el proceso de deposición.
Modelo geométrico de los substratos porosos
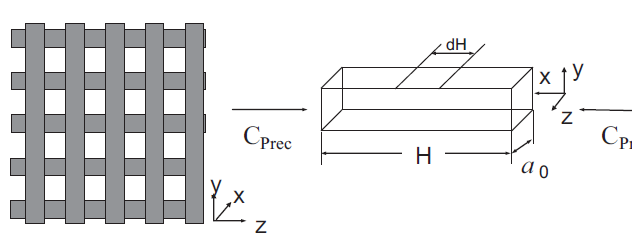
Las propiedades de las preformas a base de papel utili- zadas son únicas, ya que debido a su método de proce- samiento las fibras exhiben una orientación preferible en el eje planar y los poros resultantes son anisotrópicos. El tamaño de los poros varía desde micro- hasta mesopóricos. Esta geometría compleja gobierna el transporte de masa y la difusión de los precursores gaseosos. Para simplificar esta estructura, el modelo desarrollado se basa en la microestructura de un tejido con distribución uniforme de poros de área transversal cuadrada con altura
inicial a. y largo de poros H como se muestra en el Figu- ra 2. Por simplicidad se asume que el largo de los poros H es igual al espesor de la prueba. Los poros son abier- tos y asequibles desde los dos extremos.
Con este modelo se puede calcular el área específica superficial inicial de la preforma, que está definida como la relación entre el área superficial interior de N poros cuadrados de espesor a. sobre el volumen total de la prueba.
 [Ecn. 4]
[Ecn. 4]
Considerando que el volumen total, Vtotal, está definido como la suma entre el volumen de las fibras más el vo- lumen de espacio vacío inicial, Vporos,0, y definiendo la porosidad inicial, ., como la relación entre Vporos, . Vtotal (Ecn. 5) se puede calcular la expresión del área específi- ca superficial inicial en términos de la porosidad y las dimensiones iniciales de los poros (Ecn. 6).
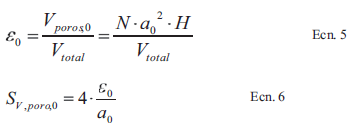 [Ecn.5 Ecn.6]
[Ecn.5 Ecn.6]Sin embargo, esta expresión es solamente válida para la preforma a condiciones iniciales. Para conocer la variación del área específica superficial, SV,poro, durante la deposición, se debe definir la función de la porosidad con respecto al área transversal variable de los poros, utilizando el cambio diferencial de la porosidad definida según Sheldon y Besmann [21] como se muestra en Ecn. 7, donde q es la probabilidad de que la capa sólida llene el poro y está definida como la porosidad momenatánea sobre la inicial.
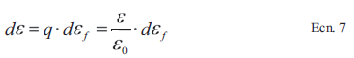 [Ecn. 7]
[Ecn. 7]La expresión de la porosidad final, f, se obtiene de su definición análoga a Ecn. 5 y reemplazando la expresión de . obtenida al despejar Ecn. 4 y reemplzar la ex-presión de SV , poro,0 de Ecn 6.
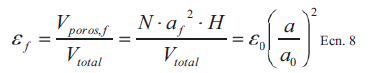 [Ecn. 8]
[Ecn. 8]Reemplazando la expresión de la porosidad final en Ecn. 7 se obtiene la expresión en Ecn. 9. Esta ecuación se integra incluyendo las condiciones iniciales a = a.y
= 0 para encontrar la expresión de la porosidad momentánea en términos de la altura del poro (Ecn. 10).}
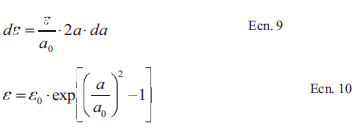 [Ecn. 9 Ecn. 10]
[Ecn. 9 Ecn. 10]Para conocer el área específica superficial momentánea, SV,poro, se asume una infiltración homogénea en todas las superficies y se realizan las siguientes operaciones ma- temáticas. La velocidad de cambio de la porosidad mo
mentánea, d /dt, se obtiene diferenciando la expresión de la porosidad con respecto al tiempo, dt, (Ecn. 11) e igualando con la expresión de Ecn. 9 al dividirla por el tiempo diferencial (Ecn. 12). Con estas transformaciones y despejando Ecn. 10 para la altura momentánea, se tie- ne la expresión del área específica superficial en función de la porosidad instantánea (Ecn. 13)
 [Ecn. 11 Ecn. 12 Ecn. 13]
[Ecn. 11 Ecn. 12 Ecn. 13]Determinación del Módulo de Thiele
Para un proceso de CVI isotérmico e isobárico el balan- ce de masa en un poro característico en un segmento diferencial está dado por la siguiente expresión:
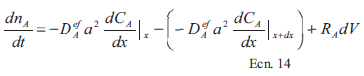 [Ecn. 14]
[Ecn. 14]donde nA es el número de moles de precursor A que atraviesa el segmento analizado, DAef es el coeficiente de difusión efectiva calculado a partir del coeficiente de difusión molecular y el coeficiente de difusión de Knud- sen según Jakubith [22], y RA.dV es el término cinético obtenido experimentalmente, donde RA es la velocidad de consumo de A con respecto al volumen de reactor
Para realizar los cálculos pertinentes se hicieron las siguientes simplificaciones:
· el sistema está en estado estacionario
· la difusión dentro de los poros transcurre de acuerdo a la 1. ley de Fick (JA= DAef. dCA/dx).
· difusión de película es despreciable
· la velocidad de la reacción catalítica se puede expresar con la expresión superficial que se ob- tuvo anteriormente
· se supone un sistema pseudo-homogéneo.
Con estas simplificaciones y reemplazando la concentración, CA y la posición axial en el poro, x, por los números adimensionales f = CA/ CA,0 y Z = x/(H/2) al dividir por la concentración en la superficie exterior del poro y el largo de infiltracón, se obtiene una expresión para el balance de masa para la concentración y posición adimensional.
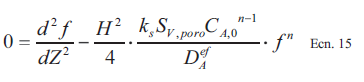 [Ecn. 15]
[Ecn. 15]Esta expresión se puede simplificar al introducir el Módulo de Thiele, , que describe la relación entre la velocidad de la reacción química y la velocidad de la difusión en los poros y para poros de área transversal cuadrados está definida por la siguiente expresión, don- de todos los valores son conocidos experiméntalo matemáticamente:
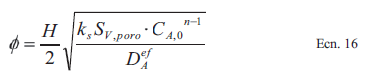 [Ecn. 1]
[Ecn. 1]Con esta definición la expresión en Ecn. 15 se simplifica a la siguiente forma:
 [Ecn. 17]
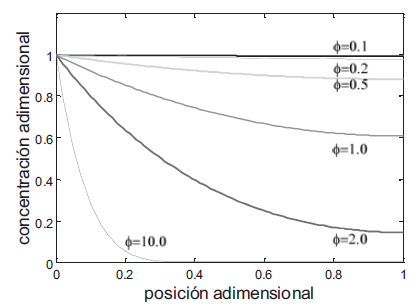
[Ecn. 17]Esta ecuación diferencial de segundo orden para un orden de reacción n diferente de uno no se puede solucio- nar matemáticamente. La expresión para la concentración adimensional, f, se obtuvo de la solución
Determinación del factor de infiltración
El factor de infiltración o factor de eficacia, , determi- na la relación entre la velocidad de reacción efectiva o real observada en el substrato poroso y la velocidad de reacción superficial esperada de acuerdo a la cinética encontrada para reacciones superficiales no porosas. Así al obtener el factor de infiltración de un proceso se conoce el grado de homogeneidad del proceso de deposición. Para poder calcular es necesario conocer entonces las velocidades de reacción superficial y efec- tiva. La velocidad de reacción superfical, r., se puede calcular fácilmente utilizando la ecuación cinética obte- nida anteriormente. Pero para obtener la velocidad de reacción efectiva¸ ref, es necesario integrar la expresión de la reacción instantánea en cada posición del poro.
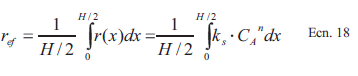 [Ecn.18]
[Ecn.18]Por lo tanto, el factor de infiltración está dado por la siguiente expresión, después de introducir la concentra- ción y la posición adimensional
La expresión para la concentración adimensional, ., se obtiene de la solución numérica como se puede observar en el Figura 3. El siguiente paso es por lo tanto, obtener el área debajo la curva de . vs. ., para el orden de reac- ción determinado anteriormente y el Módulo de Thiele calculado a partir de los datos disponibles y específico para cada caso. El área bajo la curva es el valor del fac- tor de infiltración para la reacción de deposición en los substratos estudiados.
En la Tabla 4 se encuentran los datos independientes del sistema utilizados para el cálculo de Módulo de Thiele. El coeficiente de difusión efectiva se obtiene a partir de las ecuaciones del coeficiente de difusión mo- lecular según Hirschfelder y el coeficiente de difusión de Knudsen. La porosidad inicial y final se obtienen a través de mediciones de porosimetría de mercurio (Carlo Erba Mercury Intrusion Porosimetry 2000). La altura y el largo de los poros obtienen al mediar los resultados de pruebas con SEM. Finalmente la tortuosidad se obtiene matemáticamente en función de la porosidad [1].
| Espesor de la prueba, H [cm] | 0,2 |
| Tortuosidad, [-] | 1,23 |
| Altura de los poros iniciales, a0 [µm] | 11,8 |
| Porosidad inicial, [-] | 0,9 |
| Porosidad final, [-] | 0,6 |
| Área superficial específica inicial, SV,poro,0 [1/cm] | 3,05E+03 |
| Área superficial específica final SV,poro,0,6 [1/cm] | 2,35E+03 |
En las siguientes tablas se muestran los valores numéri- cos de los diferentes parámetros para los sistemas MTS / H. y SiCl. / H.. Con estos valores fue posible calcular el Módulo de Thiele para la preforma inicial y para la pre- forma final conociendo que inicialmente la porosidad de la preforma es de 0,9, mientras que la porosidad final observada llegaba hasta a 0,6.
| Sistema | MTS / H2 | |
| mínimo | máximo | |
| Temperatura de la infiltración [°C] | 850 | 950 |
| Fracciones molares iniciales de precursor 1 [-] | 0,01 | 0,1 |
| Coeficiente de difusión molecular, Dm [cm2/s] | 4,35 – 5,02 | 5,02 |
| Coeficiente de difusión de Knudsen, Dk [cm2/s] | 1,57E+03 | 1,64E+03 |
| Coeficiente de difusión efectivo, DAef [cm2/s] | 3,16 | 3,65 |
| Concentración superficial, CA,0 [mol/cm3] | 0,17 | 1,00 |
| coeficiente cinético, ks [mol/s.(mol/cm3)1-n] | 2,66E-04 | 1,22E-03 |
| Modulo de Thiele con porosidad inicial 0, >-@ | 0,072 | 0,101 |
| Modulo de Thiele con porosidad final 0,6, >-@ | 0,063 | 0,089 |
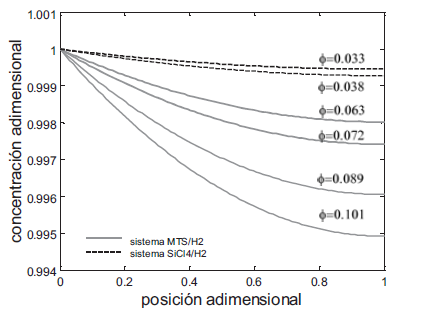
Los valores numéricos del Módulo de Thiele se encuen- tran entre 0,063 y 0,1 para el sistema de MTS / H. y entre 0,033 y 0,038 para el sistema de SiCl./H., aumen- tando en ambos casos con la temperatura y la concentra- ción de precursor. En el Figura 4 se observa el trans- curso de la concentración adimensional esperada a lo largo del poro para los dos sistemas: MTS/H. y SiCl./H., al utilizar los valores del Módulo de Thiele calculados.
| Sistema | SiCl | / H2 |
| mínimo | máximo | |
| Temperatura de la infiltración [°C] | 850 | 900 |
| Fracciones molares iniciales de precursor 1 [-] | 0,01 | 0,08 |
| Coeficiente de difusión molecular, Dm [cm2/s] | 4,39 | 4,72 |
| Coeficiente de difusión de Knudsen, Dk [cm2/s] | 1,47E+03 | 1,50E+03 |
| Coeficiente de difusión efectivo, DAef [cm2/s] | 3,19 | 3,43 |
| Concentración superficial, CA,0 [mol/cm3] | 0,11 | 0,97 |
| coeficiente cinético, ks [mol/s.(mol/cm3)1-n] | 6,83E-05 | 1,63E-04 |
| Modulo de Thiele con porosidad inicial 0, >-@ | 0,038 | 0,038 |
| Modulo de Thiele con porosidad final 0,6, >-@ | 0,033 | 0,034 |
Una vez obtenidas las curvas de la concentración adi- mensional para cada sistema, es posible obtener el factor de infiltración esperado al calcular el área bajo la curva entre 0 y 1 de las curvas de la concentración adimensio- nal a la potencia del orden de reacción obtenido en el análisis cinético (Ecn. 9). Para los sistemas estudiados y bajo las condiciones dadas se obtuvieron valores del factor de infiltración de más del 99,8% para el sistema MTS/H. y de más del 99.9% para el sistema SiCl./H..
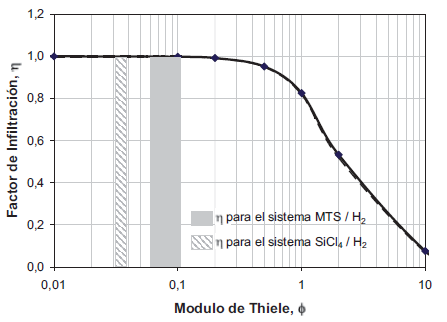
Esto también se puede ver claramente en el Figura 5 donde se muestra el transcurso del factor de infiltración esperado para diferentes valores del Módulo de Thiele. Dado que el orden de la reacción en los dos sistemas es muy parecido, las curvas de dependencia del factor de infiltración con el Módulo de Thiele son prácticamente idénticas. Para finalizar se calcula el espesor de la prue- ba máximo, o largo máximo de los poros, que se puede infiltrar homogéneamente bajo las mismas condiciones. De la gráfica y de los resultados matemáticos es posible identificar que a partir de valores del Módulo de Thiele mayores a 0,5, el valor del factor de infiltración es me- nor al 95%. Este valor se alcanza con pruebas de 1 cm de espesor. Por lo tanto, se espera que se pueda infiltrar pruebas de espesor menor a 1cm homogéneamente.
c) Caracterización de las cerámicas obtenidas
Con valores tan cercanos al 100% se concluye que la infiltración a lo largo de los poros es completamente homogénea. Esto se lo puede comprobar al analizar la estructura microscópica de las pruebas infiltradas.

Los diagramas de SEM muestran que las capas deposi- tadas son completamente homogéneas como se puede ver en el Figura 6 para el sistema MTS/H.. Sin embar- go, a pesar de que el espesor de las capas depositadas en el exterior es igual al de las depositadas en el centro de la prueba, se puede identificar una diferencia en la mor- fología de las pruebas. Esta diferencia se la debe a que en el centro la concentración de productos gaseosos (HCl) es más alta, lo que ocasiona una morfología más irregular. El espesor de las capas depositadas varía entre 2 y 3 m tanto para capas en el exterior como en el in- terior de las pruebas.
En el Figura 7 se muestra la estructura microscópica de una prueba obtenida con el sistema SiCl./H.. Se puede observar que la morfología de este depósito más bien cristalino y no tan liso. Esto se debe a las mayores tem- peraturas de deposición utilizadas con este sistema. Sin embargo, esto no afecta a que las capas depositadas sean homogéneas en toda la prueba variando entre 3 y 4 m de espesor.

Conclusiones
En este trabajo se ha logrado establecer un modelo ma- temático para predecir la homogeneidad en la infiltra- ción y deposición de cerámicas biomórficas en prefor- mas de carbono. Este modelo matemático establecido a partir del balance de masa en un poro se basa en la ciné- tica obtenida previamente en estructuras no porosas y en el modelo matemático que se definió para la geometría de preforma. Con el modelo se predijo que las preformas planas de hasta 1mm de espesor pueden ser infiltradas con los dos sistemas MTS/H. y SiCl./H. con una homo- geneidad de más de 99%, lo cual fue demostrado con micrografías de SEM donde se comparó el espesor y la morfología de las capas depositadas en estructuras infil- tradas.
Agradecimientos
La autora agradece al Departamento de Ingeniería de las Reacciones Químicas de la Friedrich-Alexander Univer- sität Erlangen-Nürnberg por el trabajo realizado en con- junto y al Ministerio de Educación e Investigación (BmBF) por la financiación consedida.
Referencias bibliográficas
1. Almeida S., D. 2004. Kinetic Investigation of the Chemical Vapor Infiltration and Reaction (CVI-R) process for the Production of SiC and TiC Biomor- phic Ceramics from Paper Preforms; Dissertation, University of Erlangen – Nuremberg.
2. de Jong, F.; Meyyappan, M. 1996. “Numerical si- mulation of silicon carbide chemical vapor deposi- tion”; Diamond and Related Materials; Vol. 5 (2); 1996; pp. 141 – 150.
3. Pritzlaff, D.; Lautner, V. 1997. CVD – Beschichtungstechnik; 1. Auflage; Eugen G. Leuzer; Verlag; Saulgau; Germany.
4. Ahmad, Z.; Mark, J.E. 1998. “Biomimetic mate- rials: recent developments in organic – inorganic hybrids”; Materials Science and Engineering C; Vol. 6; pp. 183 – 196.
5. Zhou, B. 1993. “Biomemitc Design and Test of Composite Materials”; J. of Materials Science Technology; Vol. 9; pp. 9 – 19.
6. Greil, P.; Vogli, E.; Fey, T.; Bezold A.; Popovska, N.; Gerhard, H.; Sieber, H. 2002. “Effect of Micro- structure on the fracture of biomorphous silicon carbide ceramics”; J. of the European Ceramic So- ciety; Vol. 22; pp. 2697 – 2707.
7. Greil, P.; Lifka, T.; Kaindl, A. 1998. “Biomorphic Cellular Silicon Carbide Ceramics from Wood: II. Mechanical Properties”; J. of the European Ceram- ic Society; Vol. 18; pp. 1975 – 1983.
8. Sieber, H.; Hoffmann, C.; Kaindl, A.; Greil, P. 2000. “Biomorphic Cellular Ceramics”; Advances Engineering Materials; Vol. 2 (3); pp. 105 – 109.
9. Varela-Feria, F. M.; López-Robeldo, M. J.; Martí- nez-Fernández, J.; Arellano-López, A. R. 2002. “Precursor Selection for Property Optimization in Biomorphic SiC Ceramics”; Ceramic Engineering and Science Proc.; Vol. 23 (4); pp. 681 – 687.
10. Varela-Feria, F. M.; De Arellano-Lobredo, A. R.; Martínez-Fernández, J. 2002. “Fabricación y Pro- piedades del Carburo de Silicio Biomórfico: Made- ras Cerámicas”; Boletín de la Sociedad Española de Cerámica y Vidrio; Vol. 41; pp. 377 – 384.
11. Sieber, H.; Vogli, E.; Greil, P.. 2001. “Biomorphic SiC – Ceramic Manufactured by Gas Phase Infiltra- tion of Pine Wood”; Ceramic Engineering and Science Proceedings; 22 (4, 25th Annual Confe- rence on Composites, Advanced Ceramics, Mate- rials, and Structures: B, 2001); pp. 109 – 116.
12. Vogli, E.; Sieber, H.; Greil, P. 2002. “Biomorphic SiC – ceramics prepared by Si – vapor phase infil- tration of wood”; J. of the European Ceramic So- ciety; Vol. 22; pp. 2663 - 2668
13. Greil, P.; Vogli, E.; Fey, T.; Bezold A.; Popovska, N.; Gerhard, H.; Sieber, H. 2002. “Effect of Micro- structure on the fracture of biomorphous silicon carbide ceramics”; J. of the European Ceramic So- ciety; Vol. 22; pp. 2697 – 2707.
14. Almeida Streitwieser, D., Popovska N., Gerhard, H., Emig, G. 2004. “ Application of the Chemical Vapor Infiltration and Reaction (CVI-R) Technique for the Preparation of high Porous Biomorphic SiC Ceramics Derived from Paper” ; J. of the European Ceramic Society; Vol. 25(6); pp 817-828.
15. Ohzawa, Y.; Hoshino, H.; Fujikama, M.; Nakane, K.; Sugiyama, K. 1998. “Preparation of high tem- perature filter by pressure – pulsed chemical vapor infiltration of SiC into carbonized paper – fibre pre- forms”; J. of Materials Science; Vol. 33; pp. 5259 – 5264.
16. Popovska, N., Almeida Streitwieser, D., Gerhard, H., Emig, G. 2003. “Kinetic Analysis of the Low Temperature CVD of Silicon / Silicon Carbide from Methyltrichlorosilane / Hydrogen for the Ce- ramization of Biomorphic Carbon Preforms”; in Proceedings of the Int. Symp. Chemical Vapor De- position XVI and EUROCVD 14; Vol. 1; pp. 573 – 580.
17. Popovska, N.; Almeida-Streitwieser, D.; Xu, C.; Gerhard, H.; Sieber, H. 2005. “Kinetic Analysis of the Processing of Porous Biomorphic Titanium Carbide Ceramics by Chemical Vapor Infiltration”; Chemical Vapor Deposition; Vol. 11 (3), pp 153 – 158.
18. Almeida Streitwieser, D., Popovska, N.; Gerhard, H., Emig, G. 2004. “Processing of Biomorphous SiC Ceramics from Paper Preforms by Chemical Vapor Infiltration and Reaction(CVI-R) Tech- nique”; Ceramic Engineering and Science Proceed- ings; 25 (4, 28th; Chapter 7: References 228; Inter- national Cocoa Beach Conference on Advanced Ceramics and Composites, 2004,Symposium 3)
19. Choy, K.L. 2003. “Chemical vapour deposition of coatings; Progress in Materials Science; Vol. 48; pp. 57 – 170.
20. Pierson, H. O. 1999. Handbook of Chemical Vapor Deposition (CVD): Principles, Technology and Ap- plications; 2nd edition; Noyes Publications; Wil- liam Andrew Publishing, LLC, USA.
21. Sheldon, B.W.; Besmann, T.M. 1991. “Reaction and Diffusion Kinetics During the initial Stages of Isothermal Chemical Vapor Infiltration”; Journal of American Ceramic Society; Vol. 74 (12); pp. 3046

