



Caracterización de suspensiones de nanopartículas de oro en presencia del copolímero poli (N-isopropilacrilamida)- co-poli (3-acrilamidopropil trimetilamonio). Influencia de la fuerza iónica y la temperatura
Characterization of gold nanoparticle suspensions in the presence of the poly (N-isopropylacrylamide) -co-poly (3-acrylamidopropyl trimethylammonium) copolymer. Influence of ionic strength and temperature
ACI Avances en Ciencias e Ingenierías
Universidad San Francisco de Quito, Ecuador
Recepción: 14 Septiembre 2021
Aprobación: 15 Diciembre 2021
Autor de correspondencia: dherrerarobalino1@gmail.com
Resumen: El recubrimiento de nanopartículas metálicas con polímero es de interés para dotar de estabilidad a las suspensiones de dichas nanopartículas. Por otro lado, existen polímeros termosensibles que responden de acuerdo a la temperatura a las que son expuestos. Este estudio tiene como objetivo evaluar y caracterizar el sistema conformado por nanopartículas de oro y una versión del copolímero termosensible PNIPAAM48- co-PAMPTMA6 (+). Para ello se utilizaron técnicas de dispersión dinámica de la luz, potencial zeta y espectroscopía ultravioleta-visible. El PNIPAAM48-co-PAMPTMA6 (+) fue sometido a ensayos a distintas temperaturas en los que se confirmó que la temperatura crítica inferior de disolución del copolímero es de aproximadamente 35°C y que en presencia de un medio salino tiende a agregar independientemente de la temperatura. Por otra parte, el copolímero se mezcló con nanopartículas de oro para estudiar si es un buen agente de recubrimiento y evita la agregación de las nanopartículas a elevada fuerza iónica. Se encontró que el recubrimiento de las nanopartículas de oro por parte del polímero es efectivo ya que al variar la fuerza iónica entre 0 M y 0,75 M no se observó agregación de las mismas. Esto fue corroborado por el espectro UV-visible en donde los espectros del sistema (o nanocomposite) copolímero- nanopartícula a fuerzas iónicas entre 0 M y 0,75 M son prácticamente iguales, es decir, el pico del plasmón aparece en todos los casos a la misma longitud de onda de 520 nm lo que indica que las nanopartículas de oro no han agregado. Finalmente, se estudió la evolución del sistema copolímero-nanopartícula a distintas temperaturas y fuerzas iónicas. Se detectó que tanto la influencia de la temperatura como de la fuerza iónica provocan que el sistema conjunto de copolímero-nanopartícula aumente su tamaño. Sin embargo, las nanopartículas de oro en su interior permanecen sin agregarse.
Palabras clave: nanopartículas de oro, copolímero termosensible, agregación, dispersión dinámica de la luz, potencial zeta, espectroscopia UV-vis.
Abstract: The use of polymer coating on metallic nanoparticles in order to provide great stability The use of polymer coating on metallic nanoparticles in order to provide great stability of the suspensions of nanoparticles is an important point of research. On the other hand, there are thermoresponsive polymers that respond according to the temperature to which they are exposed. This study is aimed to characterize the system made up of gold nanoparticles and a version of the thermoresponsive PNIPAAM48-b-PAMPTMA6 (+) diblock copolymer. In this study, dynamic light scattering, zeta potential and ultraviolet-visible spectroscopy were used. PNIPAAM48-b-PAMPTMA6 (+) was subjected to tests at different temperatures through which it was confirmed that the lower critical solution temperature of the copolymer is approximately 35°C and that in the presence of a saline medium it tends to increase regardless of temperature. The copolymer was mixed with gold nanoparticles to study it as a good coating agent for gold nanoparticles to avoid their aggregation at high ionic strength. The research shows that by varying the ionic strength between 0 M and 0.75 M, the coating of the gold nanoparticles by the polymer is effective since no aggregation was observed. This was corroborated by the UV-visible spectrum where the spectra of the system (or nanocomposite) copolymer-nanoparticle at ionic strengths between 0 M and 0.75 M are practically the same, i.e., the plasmon peak appears in all cases at the same wavelength of 520 nm, which indicates no aggregation of the gold nanoparticles. Finally, the evolution of the copolymer-nanoparticle system was studied at different temperatures and ionic strengths. It was detected that both the influence of temperature and ionic strength cause the copolymer-nanoparticle nanocomposite to increase its size. However, the gold nanoparticles inside remained without aggregating.
Keywords: gold nanoparticles, thermoresponsive copolymer, aggregation, dynamic light scattering, zeta potential, UV-vis spectroscopy.
INTRODUCCIÓN
En las últimas décadas, las nanopartículas de oro (AuNPs) han sido ampliamente estudiadas debido a que sus características físico-químicas las hacen aplicables en múltiples campos que van desde la biomedicina a la catálisis o la biodetección [1]. En este sentido, las AuNPs pueden ser utilizadas para el transporte selectivo de fármacos [2], para diagnóstico de enfermedades cancerígenas o para el tratamiento de tumores [3].
Para poder llevar a cabo todas esas aplicaciones es de interés el estudio de la formación de agregados de nanopartículas y de cómo prevenirlos. Esto es debido a que las soluciones coloidales son termodinámicamente inestables y tienden a flocular [4]. La comprensión adecuada del proceso de agregación de las AuNPs es fundamental, así como del proceso de estabilización. En principio, la estabilización se logra por dos mecanismos, la estabilización de carga y la estabilización estérica [5] y existen varios trabajos dedicados a tratar este tema [5-7].
El objetivo de esta investigación es caracterizar la estabilización de las soluciones de AuNPs al estar recubiertas de un copolímero termosensible. Sistemas de nanopartículas en presencia de polímeros o copolímeros han sido estudiados previamente [4,8-10] con resultados que han servido de guía para este estudio. Específicamente, el sistema (copolímero-AuNPs) PNIPAAM24-b-PAMPTMA18(+) parecido al estudiado en este trabajo, ha sido caracterizado en estudios anteriores en los cuales se concluye que, concentraciones altas del copolímero permiten una mejor estabilización estérica y electrostática de las AuNPs [5].
Para el presente estudio se planteó primero la caracterización de AuNPs individuales a distintas fuerzas iónicas y temperaturas y a continuación se caracterizó la versión utilizada del copolímero poli(N-isopropilacrilamida)-co-poli((3-acrilamidopropil) trimetilamonio, PNIPAAM48-co-PAMPTMA6 (+) que no ha sido estudiadas con anterioridad. La poli(N- isopropilacrilamida) o PNIPAAM es un polímero termosensible con una temperatura de disolución crítica inferior LCST (Lower Critical Solution Temperature) por encima de la cual las cadenas del copolímero se agregan formando estructuras micelares [11]. Esto es debido a que posee en su estructura grupos amida hidrofílicos y grupos isopropil hidrofóbicos. Temperaturas por debajo de LCST provocan un comportamiento hidrofílico del PNIPAAM mientras que temperaturas por encima de LCST provocan un comportamiento hidrofóbico pasando a formar micelas o glóbulos [12]. Así, cuando este polímero se encuentra en disolución acuosa se produce una separación de fases al calentarse por encima de su temperatura crítica LCST aproximadamente 32°C [12]. Considerando que el PNIPAAM es termosensible, la unión del mismo con las nanopartículas de oro podría influir en el comportamiento de cambio de fase provocado por la temperatura [13]. Se utilizó el copolímero PNIPAAM48-co-PAMPTMA6 (+) derivado del PNIPAAM en lugar del anterior ya que el anclaje de este en las nanopartículas de oro es más fácil debido a que la carga positiva que adquiere el copolímero en disolución le permite interaccionar fácilmente con la superficie negativa de las nanopartículas de oro comerciales utilizadas [9].
Tras la caracterización de las AuNPs y del copolímero individualmente, se procedió a la caracterización del sistema formado por ambas entidades cuando se varía la fuerza iónica y la temperatura. Para ello se utilizaron las técnicas de espectroscopía UV-visible, dispersión dinámica de la luz y potencial zeta. .
MATERIALES Y MÉTODOS
Nanopartículas de oro
En el transcurso de este estudio se han utilizado nanopartículas de oro comerciales con diámetro hidrodinámico nominal de 10 nm, aunque al ser utilizadas cuatro meses después de su compra las nanopartículas habían agregado algo y el diámetro real que determinamos mediante medidas de dispersión dinámica de luz era 20 nm. La concentración aproximada de la suspensión comercial era 6x1012 partículas/ cm3. Las nanopartículas fueron adquiridas a Sigma-Aldrich (Ref. 741957-25ML). Estas nanopartículas están recubiertas con citrato, molécula que las estabiliza al dotar a su superficie de carga negativa lo que evita en alguna medida su agregación.
Copolímero
La variante del copolímero poli(N-isopropilacrilamida)-co-poli((3-acrilamidopropil) trimetilamonio utilizada en este trabajo, PNIPAAM48-co-PAMPTMA6 (+), fue sintetizada en el Grupo del Prof. Nyström de la Universidad de Oslo a partir de PNIPAAM [11].
La Fig. 1 ilustra la estructura general de este copolímero. En la versión empleada en este trabajo, la parte correspondiente al PNIPAAM tiene una longitud de cadena n = 48 monómeros y la parte correspondiente al PAMPTMA(+) tiene una longitud de cadena m = 6 monómeros que fue sintetizada de forma exclusiva en el laboratorio del Prof. Nyström y utilizada en este trabajo por primera vez. Para abreviar la nomenclatura del copolímero a lo largo de este trabajo lo denominaremos P-48/6. El peso molecular promedio de este copolímero es 8190 g/mol.
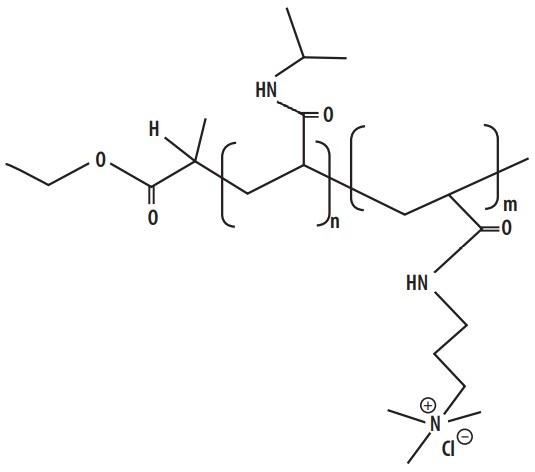
Estructura general del copolímero PNIPAAMn-co-PAMPTAm (+). En este trabajo n = 48 y m = 6
Disoluciones utilizadas
Se preparó una disolución acuosa de P-48/6 de concentración de 0,1% en peso de forma que, al añadirla a la disolución de nanopartículas, la concentración en las condiciones de trabajo era 0,075% en peso con lo cual se logra un exceso con respecto a las AuNPs que asegura el recubrimiento de éstas [9].
Por otro lado, para variar la fuerza iónica del medio, se preparó una disolución de cloruro de sodio, NaCl, de concentración 2 M a partir de la cual se prepararon las disoluciones de trabajo mediante dilución. El NaCl fue adquirido a Panreac y tenía un 99% de pureza según las especificaciones del fabricante.
Técnicas de caracterización
Espectroscopia ultravioleta-visible
La espectroscopia UV-visible se basa en caracterizar las longitudes de onda (X) en el rango ultravioleta-visible a las que absorbe radiación una molécula o partícula. En el caso de las nanopartículas metálicas, estas presentan un máximo de absorción característico, denominado pico de resonancia de plasmón superficial (SPR), que depende del tamaño de la nanopartícula. Para el caso de las AuNPs, este pico aparece en la región del visible entre el rojo y el verde.
Los espectros de absorción se realizaron con un espectrofotómetro ultravioleta-visible (UV-vis) T92+ de PG Instruments Ltd. en el cual se utilizó un rango de longitud de onda de barrido de 400 a 850 nm siendo el intervalo de barrido de 1 nm.
Dispersión dinámica de la luz (DLS)
La técnica de la dispersión dinámica de la luz es utilizada para la determinación del tamaño de las partículas en suspensión o macromoléculas en disolución. Esta técnica se basa en analizar la fluctuación a lo largo del tiempo de la intensidad de luz dispersada por las partículas a un determinado ángulo y correlacionar la rapidez de la fluctuación con el tamaño de las partículas. Las fluctuaciones son debidas al movimiento browniano aleatorio de las partículas, fenómeno explicado por Albert Einstein cuya teoría permite escribir la siguiente relación entre el coeficiente de difusión de las partículas con movimiento browniano y su tamaño,
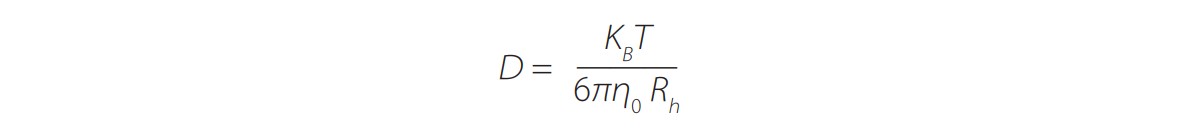 (1)
(1)donde D es el coeficiente de difusión, KB es la constante de Boltzmann, 0 la viscosidad del disolvente, T la temperatura absoluta y Rh el radio hidrodinámico de las partículas.
Esta técnica fue ampliamente desarrollada por R Pecora [14]. Las mediciones de dispersión de luz se realizaron en un equipo ZetaSizer Nano ZS (Malvern Instruments Ltd. Malvern, Reino Unido) que posee una fuente de luz láser He/Ne de 4 mW que emite a una longitud de onda de 633 nm y detecta la intensidad dispersada a un ángulo de 173°. El análisis de los datos es realizado por el software del equipo (Malvern ZetaSizer Software 7.03) el cual lleva a cabo el análisis de la función de correlación procedente de las fluctuaciones en intensidad, obtiene el coeficiente de difusión D de las partículas en suspensión y a través de la ecuación (1) relaciona este con el tamaño o radio hidrodinámico de las mismas.
Además, dicho software es capaz de proporcionar la función de distribución del tamaño hidrodinámico. La función de distribución primaria que se obtiene de la técnica de dispersión de luz es la denominada función de distribución en intensidad. Esta función de distribución informa sobre los tamaños de partícula presentes en la disolución, pero no es indicativo de sus poblaciones relativas ya que las partículas grandes dispersan mucha más luz que las pequeñas, aunque su población sea menor. Cuando aparecen muchos picos en la distribución e interesa conocer qué tamaño tiene una mayor población de partículas, el software permite, conocidos ciertos parámetros característicos de las partículas, transformar la distribución en intensidad en la denominada distribución en volumen donde la altura del pico es más proporcional a la población de partículas que presentan ese tamaño.
Aparte, en este estudio se corroboran las estimaciones del radio hidrodinámico extraídas del software mediante una aproximación con el radio de giro (Rg). Así, la ecuación (2) estima el Rg para polímero vinílicos flexibles con conformación de ovillo al azar [15],
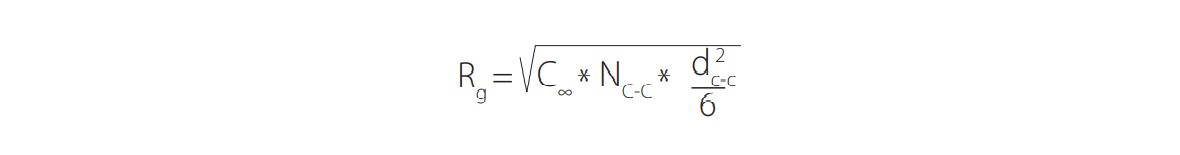 (2)
(2)donde C es la razón característica (parámetro cuyo valor depende del grado de flexibilidad del polímero), Nc-c es el número de enlaces carbono-carbono, y dc-c es la longitud del enlace carbono-carbono.
De esta manera, en el caso de estudio, el número de enlaces C-C en el esqueleto del copolímero (n=48 y m=6) es aproximadamente n + m, siendo la longitud de esos enlaces la típica del enlace simple C-C, dc-c = 0.154 nm. Como valor de C se puede tomar como aproximación razonable C = 10.6, que corresponde al C del PNIPAAM [16], puesto que la mayor parte del copolímero corresponde a este tipo de polímero.
Potencial zeta (Z)
El potencial zeta ( ) es el potencial eléctrico a cierta distancia de la superficie de una partícula o macromolécula cargada en disolución y está relacionado con la carga superficial de dicha partícula. El valor del potencial zeta es útil para evaluar la estabilidad de la suspensión de las nanopartículas. Valores próximos a cero indican que la superficie posee poca carga eléctrica por lo que las partículas pueden aproximarse y agregarla. Valores grandes (en valor absoluto) son indicativos de la estabilidad de la suspensión. Así, si el potencial zeta (en valor absoluto) es mayor que 30 mV, la suspensión se considera estable.
) es el potencial eléctrico a cierta distancia de la superficie de una partícula o macromolécula cargada en disolución y está relacionado con la carga superficial de dicha partícula. El valor del potencial zeta es útil para evaluar la estabilidad de la suspensión de las nanopartículas. Valores próximos a cero indican que la superficie posee poca carga eléctrica por lo que las partículas pueden aproximarse y agregarla. Valores grandes (en valor absoluto) son indicativos de la estabilidad de la suspensión. Así, si el potencial zeta (en valor absoluto) es mayor que 30 mV, la suspensión se considera estable.
El potencial zeta se midió en el mismo equipo que la dispersión de luz dinámica, es decir un equipo ZetaSizer Nano ZS (Malvern Instruments Ltd. Malvern, Reino Unido).
RESULTADOS Y DISCUSIÓN
En esta investigación se caracterizaron tres sistemas: (1) AuNPs a distintas fuerzas iónicas (puesto que la fuerza iónica influye en su agregación), (2) copolímero termosensible P-48/6 a distintas temperaturas (puesto que la temperatura influye en su agregación y formación de micelas) y (3) mezcla del copolímero P-48/6 con AuNPs a diferentes fuerzas iónicas y temperaturas. El objetivo principal de los ensayos es observar la interacción de las AuNPs con el P-48/6 en un rango de temperatura y en presencia y ausencia de sal.
Caracterización de AuNPs a distintas fuerzas iónicas
Las suspensiones coloidales son termodinàmicamente inestables y tienden a flocular. ingenierías En el caso de las AuNps comerciales, para evitar su agregación, estas vienen recubiertas de citrato. Al añadir sal, el recubrimiento negativo de las AuNPs es apantallado y las nanopartículas se agregan. Así, mediante las técnicas de DLS y UV-visible, se caracterizó la extensión de esta agregación a distintas concentraciones de sal transcurridas 24 horas tras la adición de sal para asegurarse de que la reacción de agregación había evolucionado de forma suficiente. La temperatura de trabajo fue 25°C.
La Fig. 2 representa la distribución de las AuNPs a distintas fuerzas iónicas entre 0 M y 1 M. A fuerzas iónicas bajas, comprendidas entre 0 M y 0,1 M la agregación se realiza de manera lenta y casi imperceptible por lo que el tamaño de las partículas formadas es similar al tamaño inicial de las AuNPs y el pico no cambia de posición. La concentración de NaCl utilizada no basta para apantallar la carga de la superficie de la nanopartícula permaneciendo estable largo tiempo. A fuerzas iónicas de 0,5 M se aprecia que las AuNPs experimentan agregación, desplazándose el pico de la función de distribución a un tamaño unas cuantas veces mayor del tamaño inicial. A fuerzas iónicas de 0,75 M y 1 M, el pico de la distribución de tamaño se desplaza a valores superiores a 100 nm, indicando una fuerte agregación. De hecho, a valores de fuerza iónica superiores a 0,75 M los agregados alcanzan un tamaño límite que hacen que precipiten rápidamente. Dicha precipitación se apreciaba claramente a fuerza iónica 1 M (a las 24 horas la mayoría de los agregados habían ya precipitado). En base a esto se eligió la fuerza iónica 0,75 M como límite en este estudio.
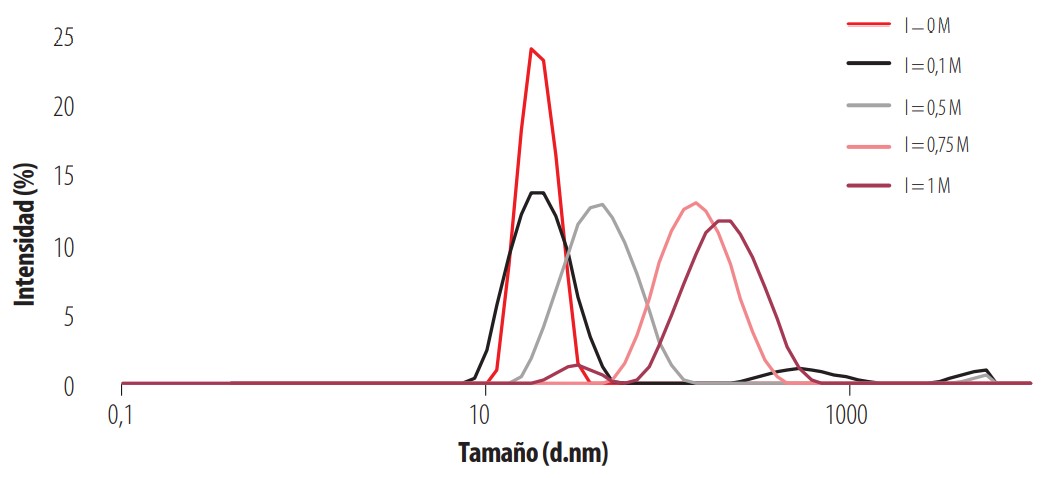
En la Fig. 3 se muestra el análisis de UV-visible que confirma las conclusiones anteriores. A fuerzas iónicas bajas, 0 M y 0,1 M la longitud de onda correspondiente al máximo de absorbancia es siempre la misma y muy cercana a 520 nm, lo que corresponde a AuNPs con tamaños inferiores a 50 nm (cuyas suspensiones presentan un característico color rojo [17]). Este resultado indica que no existe agregación apreciable de las nanopartículas en ese rango de fuerza iónica. Por el contrario, a una fuerza iónica de 0,75 M se observa claramente el desplazamiento del pico del plasmón a valores mayores de longitud de onda, así como su ensanchamiento lo que es indicativo de que se han formado agregados de gran tamaño. Esto se evidencia en la pérdida de la coloración roja típica de las suspensiones de AuNPs de 20 nm, pasando la suspensión a una coloración más bien púrpura, indicador de que las nanopartículas han agregado aumentando de tamaño.
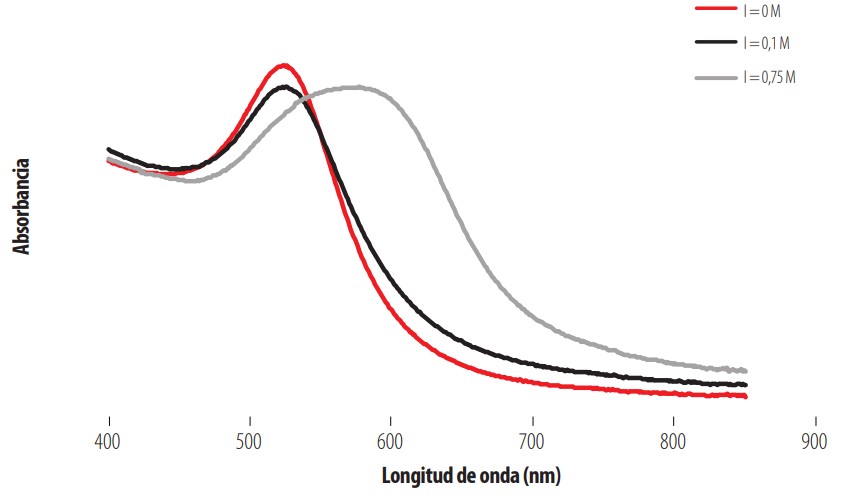
Espectro UV-visible para AuNPs a distintas fuerzas iónicas
Caracterización del copolímero P-48/6 a distintas temperaturas
La influencia que puede tener la temperatura en el comportamiento del copolímero es el objeto de estudio en este apartado. Para ello se preparó una disolución de copolímero P-48/6 de concentración 0,01% en peso sin sal añadida (fuerza iónica cero, I = 0 M). Para caracterizar el copolímero se utilizó una concentración pequeña (diez veces inferior a la concentración preparada inicialmente y utilizada luego para recubrir las nanopartículas) para evitar que las cadenas agreguen debido a las interacciones producidas por la elevada concentración y no simplemente por efecto de la temperatura. Así, una elevada concentración conlleva una excesiva turbidez cuando se alcanza la temperatura LCST que impide una buena medición de la intensidad de luz dispersada.
La evolución del tamaño del copolímero con la temperatura en un rango de temperaturas entre 25°C y 55°C se estudió mediante la técnica de dispersión de la luz. A pesar de la baja concentración utilizada para el copolímero (más pequeña no es posible porque no da buena señal), a cualquier temperatura se producen interacciones entre las cadenas y, por tanto, agregados, por lo que la distribución en intensidad presenta picos a muchos tamaños. Para dilucidar qué picos (qué tamaños) son realmente importantes a cada temperatura se ha representado la distribución en volumen (Fig. 4). Así, en la Fig. 4 se observa que a 25°C y a 35°C las cadenas de polímero están poco o nada agregadas, lo que significa que a estas temperaturas predomina el carácter hidrofílico del copolímero y ésta está bien disuelto. De hecho, los picos de la distribución aparecen en torno a 3 nm que corresponde al tamaño que tendrían las cadenas individuales del copolímero en disolución. Este valor se puede estimar considerando la ecuación (2) para el radio de giro Rg. Efectuando los cálculos se obtiene que el valor del Rg es de 1,5 nm, es decir, un diámetro (valor representado en Fig. 4) de 3 nm.
A partir de 35°C existe la presencia sólo de agregados (los picos de la Fig. 4 aparecen en torno a 500 nm). Esto es lógico puesto que a temperaturas superiores a la LCST en la cadena de copolímero predomina el carácter hidrofóbico, provocando la formación de redes o agregados de polímero debido a interacciones entre los segmentos hidrofóbicos.
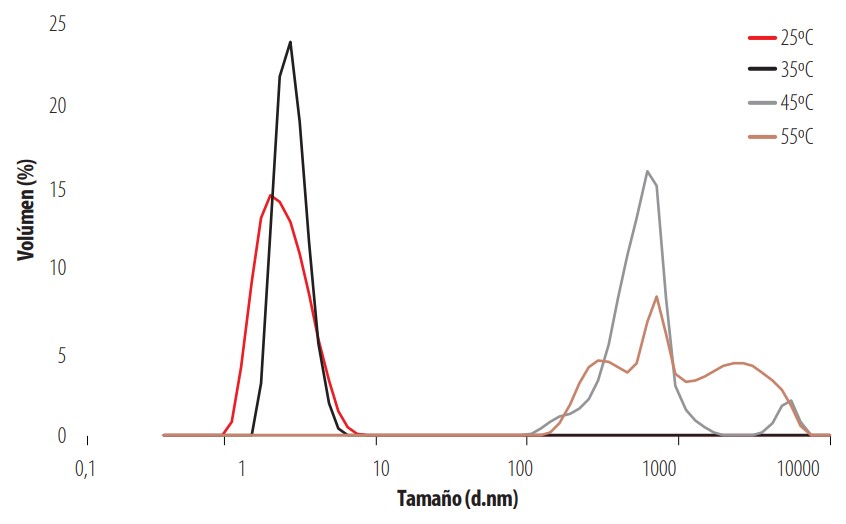
Distribución de tamaños en volumen del copolímero P-48/6 a distintas temperaturas con I = 0 M
Caracterización del nanocomposite (AuNPs + P-48/6) a distinta fuerza iónica
Para lograr el recubrimiento de las AuNPs con el copolímero se mezclaron 0,5 ml de disolución comercial de AuNPs y 1,5 ml de disolución P-48/6 de 0,1% en peso con lo que la concentración de trabajo del copolímero fue 0,075% en peso. Esta disolución fue analizada por medio de las técnicas de DLS, UV-visible y potencial zeta.
Para facilitar la comparación de los tres sistemas estudiados, en la Fig. 5 se representan conjuntamente las funciones de distribución en volumen de las disoluciones iniciales de AuNPs, P-48/6, y nanocomposite (AuNPs + P-48/6) a la temperatura de 25°C y en ausencia de sal añadida (I = 0). Se aprecia el pico del P-48/6 en torno a 3 nm, el pico de las AuNPs originales en torno a 20 nm y el pico del nanocomposite a un tamaño algo mayor que el de las AuNPs individuales, en torno a 50 nm. Una interpretación puede ser que las cadenas de copolímero interaccionan con las nanopartículas de oro y las recubren generando una estructura de mayor tamaño que la AuNPs individuales. También pueden existir pequeñas redes de copolímero que atrapen nanopartículas en su seno.
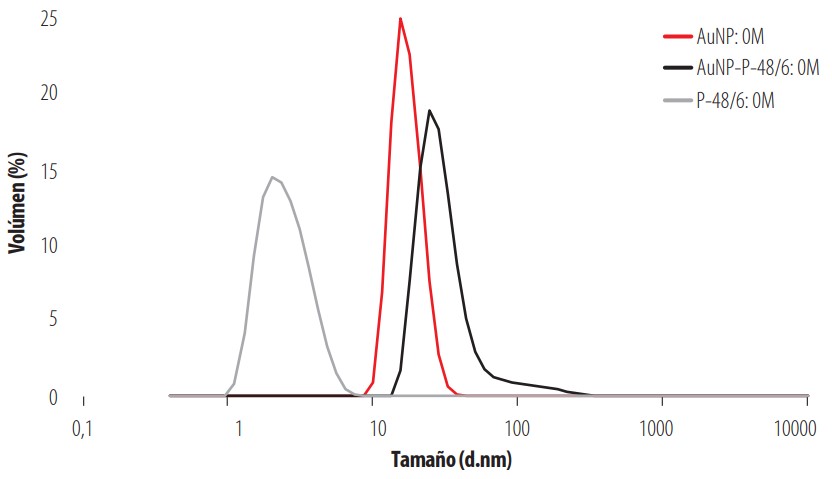
Comportamiento de AuNPs, (AuNPs. P-48/6) y P-48/6 a I = 0 M y a 25°C
La Fig. 6 corresponde a las funciones de distribución en intensidad de las disoluciones de AuNPs, P-48/6 y del nanocomposite (AuNPs + P-48/6) a la fuerza iónica límite I = 0,75 M y a 25°C. Como ya se vio en las Fig. 2 y 3, las AuNPs individuales agregan en presencia de sal, apareciendo tamaños en torno a 200 nm. Por otro lado, el copolímero a I = 0,75 M está principalmente en forma de agregados y no hay cadenas individuales (no aparece pico en torno a 3 nm). Aunque la temperatura es inferior a la LCST, la concentración de trabajo es elevada y la presencia de sal apantallando la carga del copolímero facilita que las cadenas de éste se asocien. Cuando se forma el nanocomposite, en el sistema AuNPs + P-48/6, estas redes de copolímero que se forman a elevada fuerza iónica, atrapan todas las AuNPs en su interior por lo que la función de distribución del sistema AuNPs + P-48/6 está formada por picos a partir de 100 nm (si hubiera AuNPs libres habría un pico a 20 nm en la función de distribución). El tamaño de estas redes de copolímero con AuNPs atrapadas es algo menor que las redes formadas solamente por P-48/6 solo. Esto se puede explicar porque las AuNPs atrapadas (carga negativa) producen un apantallamiento extra de la carga positiva de las cadenas de copolímero que forma la red con lo que la red puede encogerse algo más.
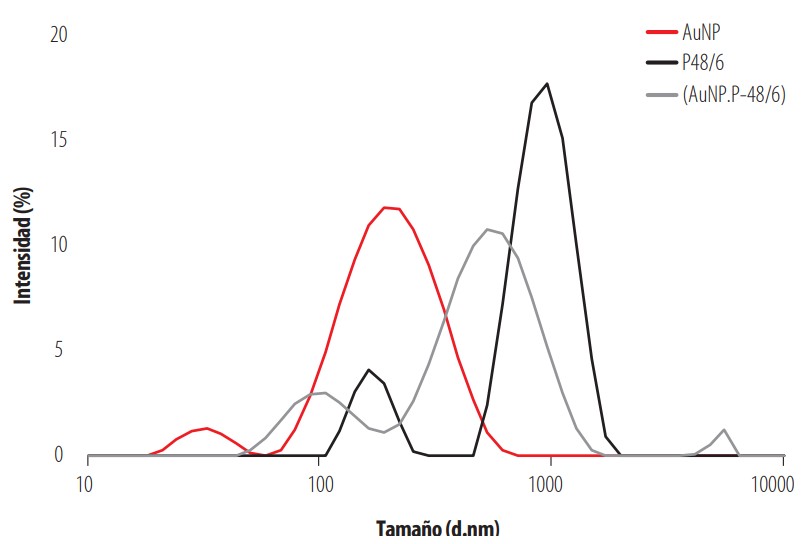
Distribución de intensidad de AuNPs, (AuNPs. P-48/6) y P-48/6 a I = 0,75M, 25°C
Finalmente, es importante determinar si las AuNPs que forman parte del nanocomposite se encuentran agregadas en presencia de sal. La Fig. 7 recoge los espectros UV-vis de las disoluciones de las AuNPs individuales y del nanocomposite tanto en presencia como en ausencia de sal. Se aprecia que la longitud de onda a la que aparece el pico de plasmón en el nanocomposite (AuNPs + P-48/6) tanto a fuerza iónica 0 M como 0,75 M es aproximadamente la misma e igual a la longitud de onda del pico de plasmón característico de las AuNPs sin agregar a I = 0 M, (el copolímero no da señal UV-visible), es decir aproximadamente 520 nm. De esta manera se puede afirmar que, si bien el copolímero agrega con la sal, las AuNPs permanecen sin formar agregados, atrapadas e inmovilizadas individualmente en la red de copolímero.
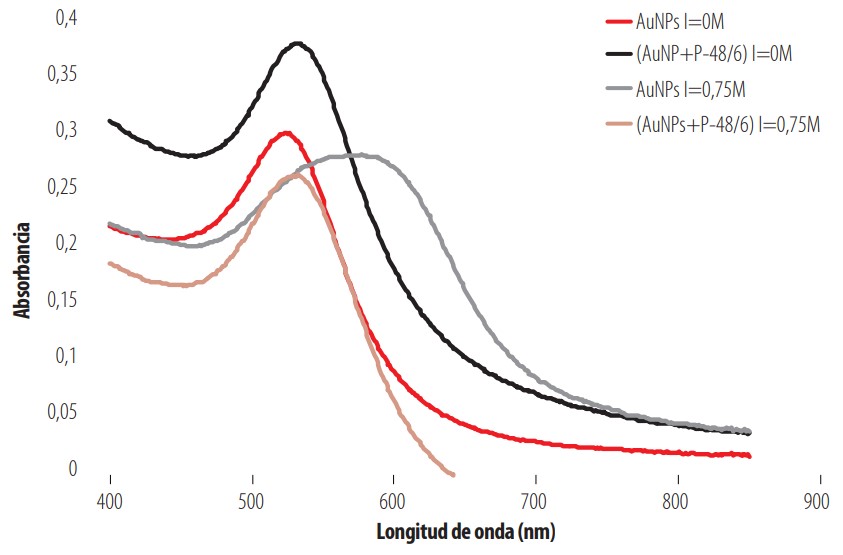
Espectro UV-visible de AuNPs y (AuNPs. P48/6) a 25oC y a I = 0 M y 0,75 M
Ciertamente, el pico del sistema (AuNPs + P-48/6) a I=0.75 M está ligeramente desplazado a longitudes de onda mayores respecto del pico de las AuNPs individuales, pero esto puede achacarse a que muchas de las nanopartículas atrapadas en la red polimérica se encuentran suficientemente próximas (sin llegar a agregar). La agregación de las AuNPs, por otro lado, es clara, como ya se puso de manifiesto en la Fig. 3, cuando se añade sal sin que esté el copolímero presente.
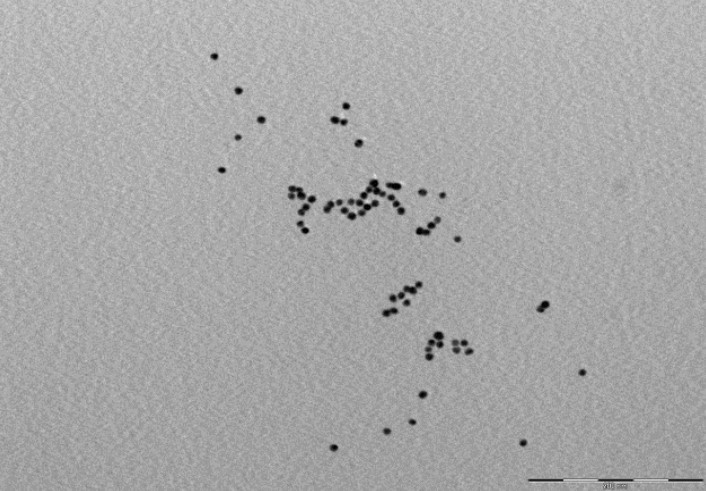
Imagen TEM del nanocomposite a I = 0 M. Escala de 200 nm
Las afirmaciones anteriores son apoyadas por imágenes de microscopía de transmisión de electrones TEM. estas arrojan luz sobre el comportamiento de las AuNPs dentro del endone copolímero. Las Fig 8 es una imagen TEM correspondiente a una fuerza iónica I=0 M. En ella se nota claramente que las AuNPs se encuentran en forma dispersa, asociadas en su mayoría a cadenas de polímero individuales.
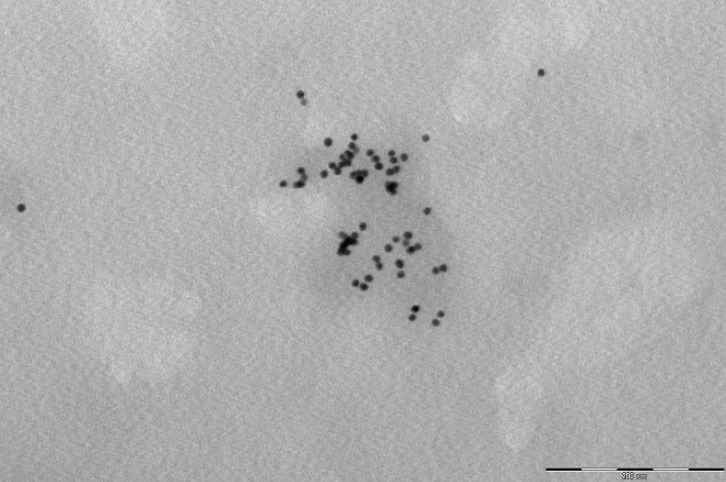
Imagen TEM del nanocomposite a I = 0,75 M. Escala de 200 nm
Cuando la fuerza iónica es I = 0,75 M, obtenemos la imagen TEM mostrada en la Fig 9 donde se aprecia que las AuNPs siguen sin agregar, aunque aparecen menos dispersas que anteriormente. Esto último puede explicarse debido a que el copolímero, al estar expuesto a una fuerza iónica elevada, se encuentra formando marañas compactas, razón por la cual en la imagen se observa que las AuNPs impregnadas en estas marañas se encuentran muy juntas entre sí, pero conservan su individualidad.
Caracterización del nanocomposite (AuNPs + P-48/6) a distinta temperatura
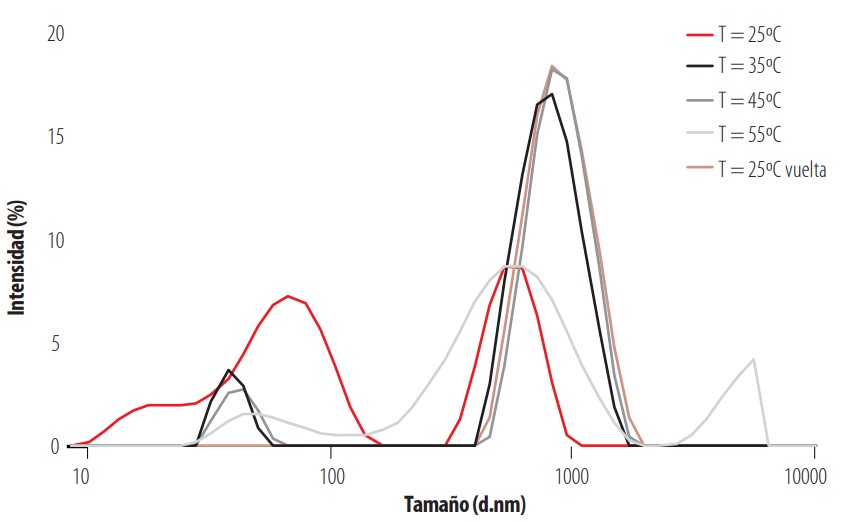
Distribución de tamaño del (AuNPs. P-48/6) a distintas temperaturas con fuerza iónica de 0,75 M
Ya que el copolímero es termosensible, se estudió el comportamiento del sistema (AuNPs + P48/6) al variar la temperatura entre 25°C y 55°C fijando la fuerza iónica en el valor límite de 0,75 M. En la Fig. 10 se representa la distribución en intensidad del tamaño del nanocomposite para las distintas temperaturas consideradas.
A 25°C la distribución es la misma que ya aparecía en la Fig. 6. Al aumentar la temperatura en el rango de 35°C a 55°C, se observa que la distribución se desplaza a tamaños mayores. Esto es coherente con la LCST confirmada en este estudio. Es decir, a temperaturas de 35°C y 55°C el copolímero adquiere un carácter hidrofóbico global y tiende agregar, aún más de lo que ya estaba debido a la fuerza iónica. Luego, al parecer, tanto la temperatura como la fuerza iónica influyen en el tamaño del nanocomposite, observando un mayor tamaño a I = 0,75 M.
En la Fig. 10 también se ha representado la distribución obtenida a 25°C tras dejar enfriar la muestra (25°C vuelta), aproximadamente una hora después de terminar con el ensayo a 55°C. Se observa que, al dejar pasar un cierto tiempo, el nanocomposite empieza a disminuir su tamaño (picos se desplazan a tamaños menores) lo cual indica que está ocurriendo un proceso de desagregación de los agregados formados entre las cadenas del copolímero por efecto de la temperatura.
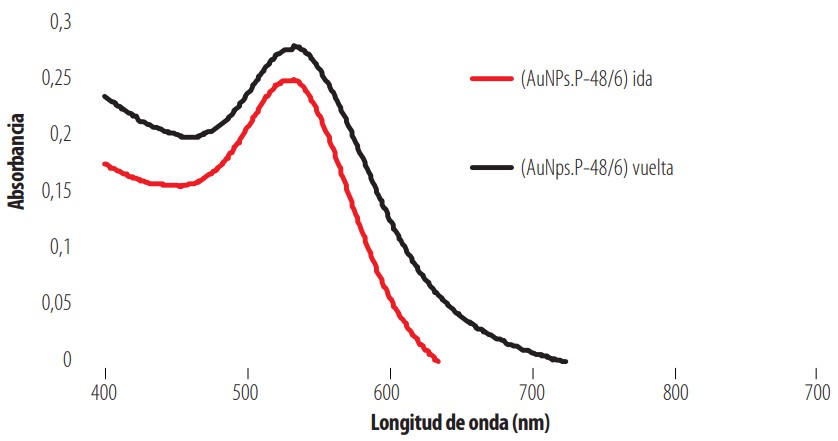
Espectro UV-visible de (AuNPs. P48/6) a temperaturas de 25oC en ida y vuelta con I = 0,75 M
Ahora bien, que el sistema (AuNPs + P-48/6) haya agregado a temperaturas superiores a la LCST no nos aclara lo sucedido con las AuNPs atrapadas en su interior. Ante la imposibilidad de llevar a cabo un análisis de UV-visible a distintas temperaturas con la instrumentación utilizada, se procedió a caracterizar el estado de las AuNPs a 25°C tanto al inicio de la rampa de temperatura (ida) como tras el proceso de enfriamiento (vuelta). La Fig. 11 recoge los espectros obtenidos en ambas situaciones. Se aprecia que las AuNPs mantienen en todo momento su pico de plasmón a 520 nm aproximadamente, tanto antes de iniciarse la rampa de temperatura como después. Esto evidencia que las AuNPs no se encuentran agregadas sino simplemente atrapadas en las redes formadas por las cadenas del copolímero.
Estudio del potencial zeta (Z)
Se utilizó la medida del potencial zeta para determinar la estabilidad de las suspensiones de las AuNPs solas, del copolímero y del sistema (AuNPs + P-48/6). Las mediciones se realizaron a 25°C y a fuerzas iónicas nula y 0,05 M (la fuerza iónica ha de ser pequeña porque una fuerza iónica excesiva implica una elevada conductividad que estropea los electrodos de la celda de trabajo). Los experimentos se llevaron a cabo en el mismo equipo que se utilizó para las medidas de DLS.
Así, si el potencial zeta presenta valores muy positivos o muy negativos, las partículas coloidales tienden a repelerse y la suspensión es estable. Se asume que valores de potencial zeta por debajo de -30 mV y por encima de +30 mV confieren estabilidad a la suspensión coloidal. Si el potencial zeta se encuentra entre estos valores, las suspensiones coloidales serán inestables y tienden a agregarse.
En la Fig. 12 se representan en forma de diagrama de barras las medidas del potencial zeta llevadas a cabo para las AuNPs, el P-48/6 y el nanocompsite (AuNPs + P-48/6). En las AuNPs a fuerza iónica 0 M, el potencial zeta tiene valores de -30 mV, por tanto, se pone de manifiesto la estabilidad de las mismas. Por el contrario, si se aumenta la fuerza iónica a 0,05 M, el potencial zeta tiende hacia cero con lo que las AuNPs serán menos estables y empezarán a agregar. Estos valores son consecuentes con lo observado en el DLS y UV-visible para las AuNPs.
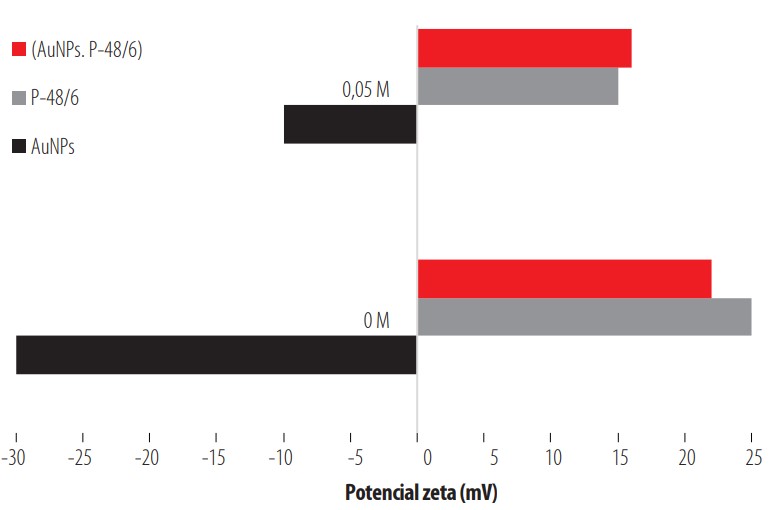
Medidas del potencial zeta
El P-48/6, que es de naturaleza catiónica, tiene un potencial zeta positivo de 25 mV a I = 0 M, lo que implica una relativa estabilidad del copolímero al ser el potencial muy cercano a 30 mV. En cambio, al aumentar la fuerza iónica, el potencial zeta disminuye con lo que aumenta la tendencia del copolímero a formar agregados. Esto es coherente con el comportamiento observado en los experimentos de DLS.
Finalmente, los valores del potencial zeta para el nanocomposite (AuNPs + P-48/6) son perfectamente coherentes con los resultados procedentes de las medidas de DLS y UV- visible. A I = 0 M ya se tiene un valor menor que 30 mV, es decir el nanocomposite tiene cierta inestabilidad como se evidenció en la Fig. 6 donde se pone de manifiesto la presencia de agregados (aunque son agregados de copolímero, no de nanopartículas como se discutió anteriormente). Por otro lado, al aumentar la fuerza iónica, como se esperaba por los análisis previos, el nanocomposite (AuNPs + P-48/6) pierde estabilidad formando agregados mayores.
CONCLUSIONES
Las nanopartículas de oro tienden a perder su estabilidad y agregarse al aumentar la fuerza iónica de la suspensión en la que se encuentran. La distribución de tamaño y el desplazamiento del pico de plasmón obtenidos a través de las técnicas DLS y UV-visible ponen de manifiesto este fenómeno de agregación. Se pudo determinar que a fuerzas iónicas mayores de 0,75 M (utilizando como electrolito de NaCl) la suspensión pierde su estabilidad en un tiempo inferior a un día y las nanopartículas agregadas precipitan.
La temperatura LCST del copolímero PNIPAAM48-co-PAMPTMA6 (+), o P-48/6, es aproximadamente 35°C. Por encima de esa temperatura, las funciones de distribución de tamaño obtenidas mediante DLS se desplazan a tamaños mayores que los correspondientes a cadenas individuales. Esto es debido al aumento del carácter hidrofóbico del segmento de PNIPAAM que provoca la agregación de las cadenas. Además, en presencia de sal, el copolímero P-48/6 tiende a formar redes. Esto implica que, aún a temperaturas inferiores a la LCST, cuando el carácter hidrofílico predomina, el copolímero agrega. Así que, el copolímero no sólo es termosensible sino también susceptible a la fuerza iónica.
En el nanocomposite (AuNPs + P-48/6) a fuerza iónica 0,75 M, las nanopartículas permanecen sin agregar, atrapadas en el interior de una red formada por diversas cadenas de copolímero como pone de manifiesto la utilización conjunta de las técnicas de DLS y espectroscopia UV-visible. Al aumentar la temperatura de la disolución, el copolímero adquiere carácter hidrofóbico a temperaturas superiores a 35°C, favoreciéndose las interacciones copolímero-copolímero y el consecuente desplazamiento de la función de distribución a tamaños mayores. Sin embargo, el pico de plasmón permanece en el mismo valor de longitud de onda correspondiente a las AuNPs originales (520 nm). Por tanto, tras aumentar la temperatura y la fuerza iónica en el nanocomposite (AuNPs + P-48/6), las AuNPs permanecen en forma individual atrapadas y protegidas por la red de copolímero.
Finalmente, en principio, el copolímero PNIPAAM48-co-PAMPTMA6 (+) podría ser utilizado para recubrir y estabilizar otro tipo de nanopartículas metálicas debido a que cualquier nanopartícula con carga superficial negativa es susceptible de interaccionar con el copolímero de carga positiva.
AGRADECIMIENTOS
JGHC quiere agradecer al Prof. B. Nyström de la Universidad de Oslo el suministro del copolímero utilizado y a la Fundación Séneca de la CARM (España) la concesión del proyecto 20933/PI/18.
CONTRIBUCIÓN DE LOS AUTORES
David Herrera Robalino: concepción de la investigación, diseño de la metodología, curación de datos para la investigación, análisis e interpretación de datos, redacción del manuscrito
José Ginés Hernández Cifre: concepción de la investigación, diseño de la metodología, curación de datos para la investigación, análisis e interpretación de datos, redacción del manuscrito, revisión crítica del contenido intelectual del manuscrito.
CONFLICTO DE INTERÉS
Los autores declaran no tener ningún conflicto de intereses. Los patrocinadores no tuvieron ningún papel en el diseño del estudio; en la recopilación, análisis o interpretación de datos; en la redacción del manuscrito o en la decisión de publicar los resultados.
Referencias
Dondapati, S. K., Sau, T. K., Hrelescu, C., Klar, T. A., Stefani, F. D., & Feldmann, J. (2010). Label-free Biosensing Based on Single Gold Nanostars as Plasmonic Transducers. ACS Nano, 4(11), 6318-6322. doi: https://doi.org/10.1021/nn100760f
Rastogi, L., Kora, A. J., & Arunachalam, J. (2012). Highly stable, protein capped gold nanoparticles as effective drug delivery vehicles for amino-glycosidic antibiotics. Materials Science and Engineering C, 32(6), 1571-1577. doi: https://doi.org/10.1016/j.msec.2012.04.044
Zhang, X. (2015). Gold Nanoparticles: Recent Advances in the Biomedical Applications. Cell Biochemistry and Biophysics, 72(3), 771-775. doi: https://doi.org/10.1007/s12013-015-0529-4
Pamies, Ramón, Cifre, J. G. H., Espín, V. F., Collado-González, M., Baños, F. G. D., & De La Torre, J. G. (2014). Aggregation behaviour of gold nanoparticles in saline aqueous media. Journal of Nanoparticle Research, 16(4). doi: https://doi.org/10.1007/s11051-014-2376-4
[5] Pamies, Ramón, Zhu, K., Volden, S., Kj0niksen, A. L., Karlsson, G., Glomm, W. R., & Nyström, B. (2010a). Temperature induced flocculation of gold particles with an adsorbed thermoresponsive cationic copolymer. Journal of Physical Chemistry C, 114(50), 21960-21968. doi: https://doi.org/10.1021/jp106520k
Napper, D. H., & Netschey, A. (1971). Studies of the Steric Stabilization of Colloidal Particles. Journal of Colloid and Interface Science, 37(3), 528-535. doi: https://doi.org/10.1016/0021-9797(71)90330-4
[7] Yavuz, M. S., Cheng, Y., Chen, J., Cobley, C. M., Zhang, Q., Rycenga, M., Xie, J., Kim, C., Song, K. H., Schwartz, A. G., Wang, L. V, & Xia, Y. (2009). Gold nanocages covered by smart polymers for controlled release with near-infrared light. Nature Materials, 8(12), 935-939. doi: https://doi.org/10.1038/nmat2564
Collado-González, M., Fernández Espín, V., Montalbán, M. G., Pamies, R., Hernández Cifre, J. G., Díaz Baños, F. G., Víllora, G., & García de la Torre, J. (2015). Aggregation behaviour of gold nanoparticles in presence of chitosan. Journal of Nanoparticle Research, 17(6). doi: https://doi.org/10.1007/s11051-015-3069-3
Fernandez Espin, V. (2017). Técnicas instrumentales y computacionales para la caracterización de sistemas de macromoléculas y nanopartículas. Implementación y aplicaciones [Tesis de Doctorado]. En Universidad de Murcia. doi: https://doi.org/10.13140/RG.2.1.2171.2482
Zhu, K., Jin, H., Kj0niksen, A. L., & Nyström, B. (2007). Anomalous transition in aqueous solutions of a thermoresponsive amphiphilic diblock copolymer. Journal of Physical Chemistry B, 111(37), 10862-10870. doi: https://doi.org/10.1021/jp074163m
Bayati, S., Zhu, K., Trinh, L. T. T., Kj0niksen, A. L., & Nyström, B. (2012). Effects of temperature and salt addition on the association behavior of charged amphiphilic diblock copolymers in aqueous solution. Journal of Physical Chemistry B, 116(36), 11386-11395. doi: https://doi.org/10.1021/jp306833x
[12] Schild, H. G. (2003). Poly(N-isopropylacrylamide): experiment, theory and application. Progress in Polymer Science, 17(2), 163-249. doi: https://doi.org/10.1016/0079-6700(92)90023-r
[13] Zhu, M. Q., Wang, L. Q., Exarhos, G. J., & Li, A. D. Q. (2004). Thermosensitive Gold Nanoparticles. Journal of the American Chemical Society, 126(9), 2656-2657. doi: https://doi.org/10.1021/ja038544z
Pecora, R. (1964). Doppler shifts in light scattering from pure liquids and polymer solutions. The Journal of Chemical Physics, 40(6), 1604-1614. doi: https://doi.org/10.1063/1.1725368
Pamies, R, Cifre, J. G. H., & De La Torre, J. G. (2007). Brownian dynamics simulation of polyelectrolyte dilute solutions under shear flow. Journal of Polymer Science, Part B: Polymer Physics, 45(1), 1-9. doi: https://doi.org/10.1002/polb.20994
Zeng, F., Tong, Z., & Sato, T. (1999). Molecular chain properties of poly (N-isopropyl acrylamide). Science in China, Series B: Chemistry, 42(3), 290-297. doi: https://doi.org/10.1007/BF02874245
Sztandera, K., & Gorzkiewicz Michatand Klajnert-Maculewicz, B. (2018). Gold Nanoparticles in Cancer Treatment. doi: https://doi.org/10.1021/acs.molpharmaceut.8b00810